心筋前駆細胞ACMsの生理的意義と心臓に存在する細胞の立体的相互関係の解明
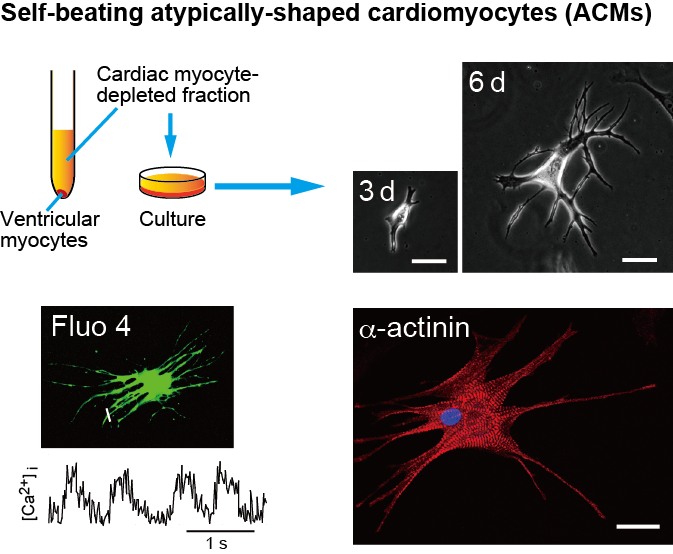
成体マウスの心室組織から調製した「心筋細胞を除いた分画」中 に,培養数日後から自発的に大きく成長し拍動を始める細胞が存在することを発見し,その特徴的な形態からatypically-shaped cardiomyocytes(ACMs)として同定しました。ACMsは,自動性をもち,収縮タンパク質,イオンチャネル,分泌物質の発現の解析から, ペースメーカー細胞,心房筋細胞,心室筋細胞のそれぞれの特徴を示すことがわかり,虚血耐性が高いことなどから未分化な心筋細胞に分類されました。また, ACMsは,新 生仔から老齢にいたるマウスの心臓に存在することから胎児性心筋細胞に由来する心筋前駆細胞の一種であると推察されます。一方,ヒト心筋組織においても老 齢にいたるまで心室筋組織中に存在する ことを見いだし,ACMsの生理的意義の解明と,心筋細胞再生における応用の可能性について検討しています。
また,このような心筋前駆細胞を初めとする心臓に存在する種々の細胞について,その局在を立体的に構築し相互関係を解明するため,心臓組織を透明化して,タンパク質発現の3D画像解析をする技術の確立を目指しています。
文責: 尾松万里子(Mariko Omatsu-Kanbe)
心臓ペースメーカー電位および心房筋K+チャネルの機能調節
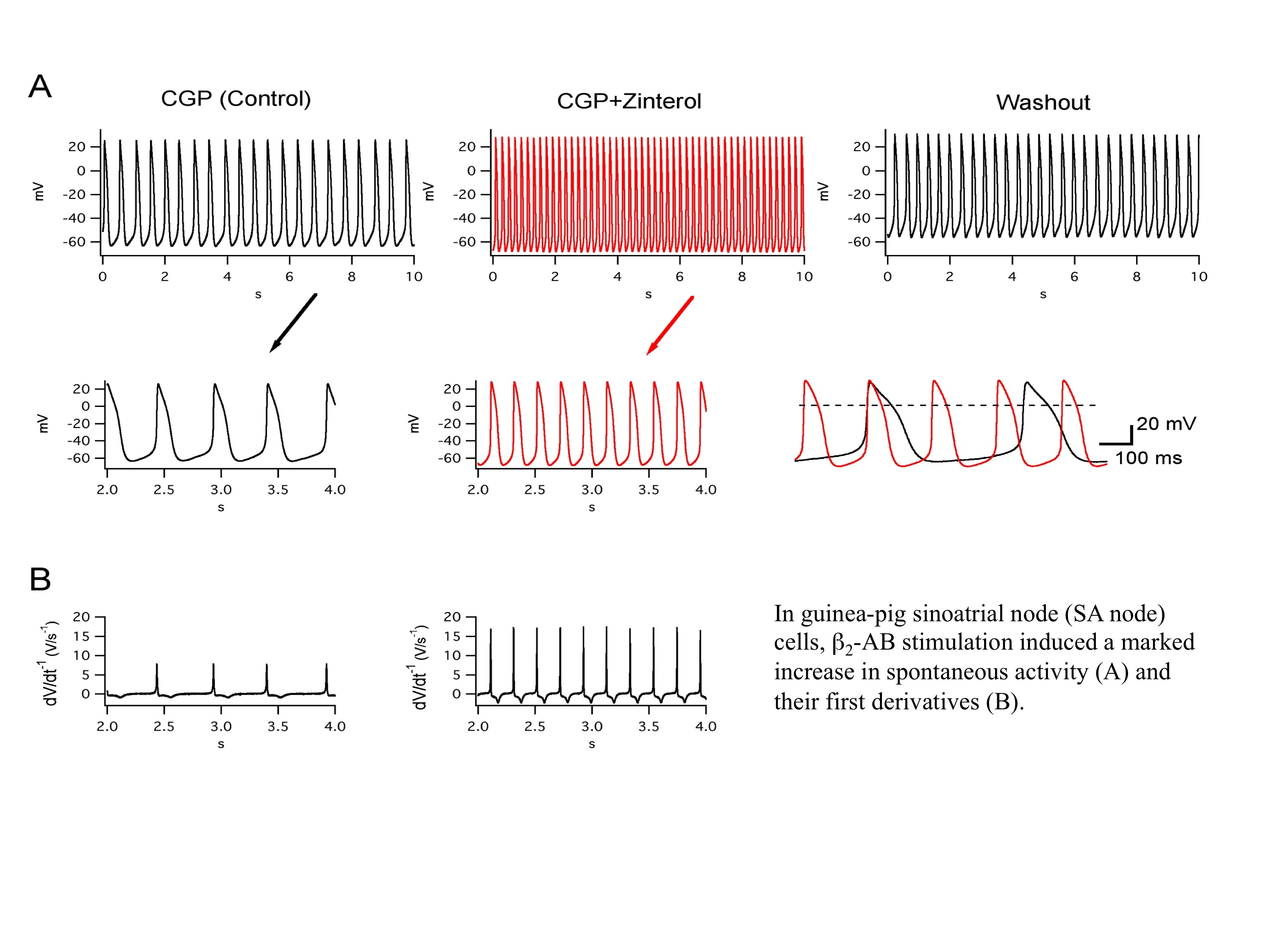
心臓は、洞房結節にあるペースメーカー細胞の生み出す信号に応じて律動的に収縮と弛緩を行い、体に血液を送っています。一方、交感神経および迷走神経の 緊張は常に心拍数や心収縮力を変化させますが、これは神経終末から放出される神経伝達物質が心筋に発現する種々のイオンチャネルの機能を調節するためであ ります。私たちはモルモットから単離された洞房結節細胞よりペースメーカー電位を記録し、交感神経緊張時に対応するβ2受容体刺激の調節作用を研究してい ます。また心臓には外向き電流を通す数種類のK+チャネルがあり、その内、2種類の遅延整流性K+チャネル(IKr, IKs)はペースメーカー電位の再分極の形成に非常に重要であります。現在β受容体が刺激された条件下でペースメーカー電位の調節におけるこれらのK+チャネルの関わりについても調べています。
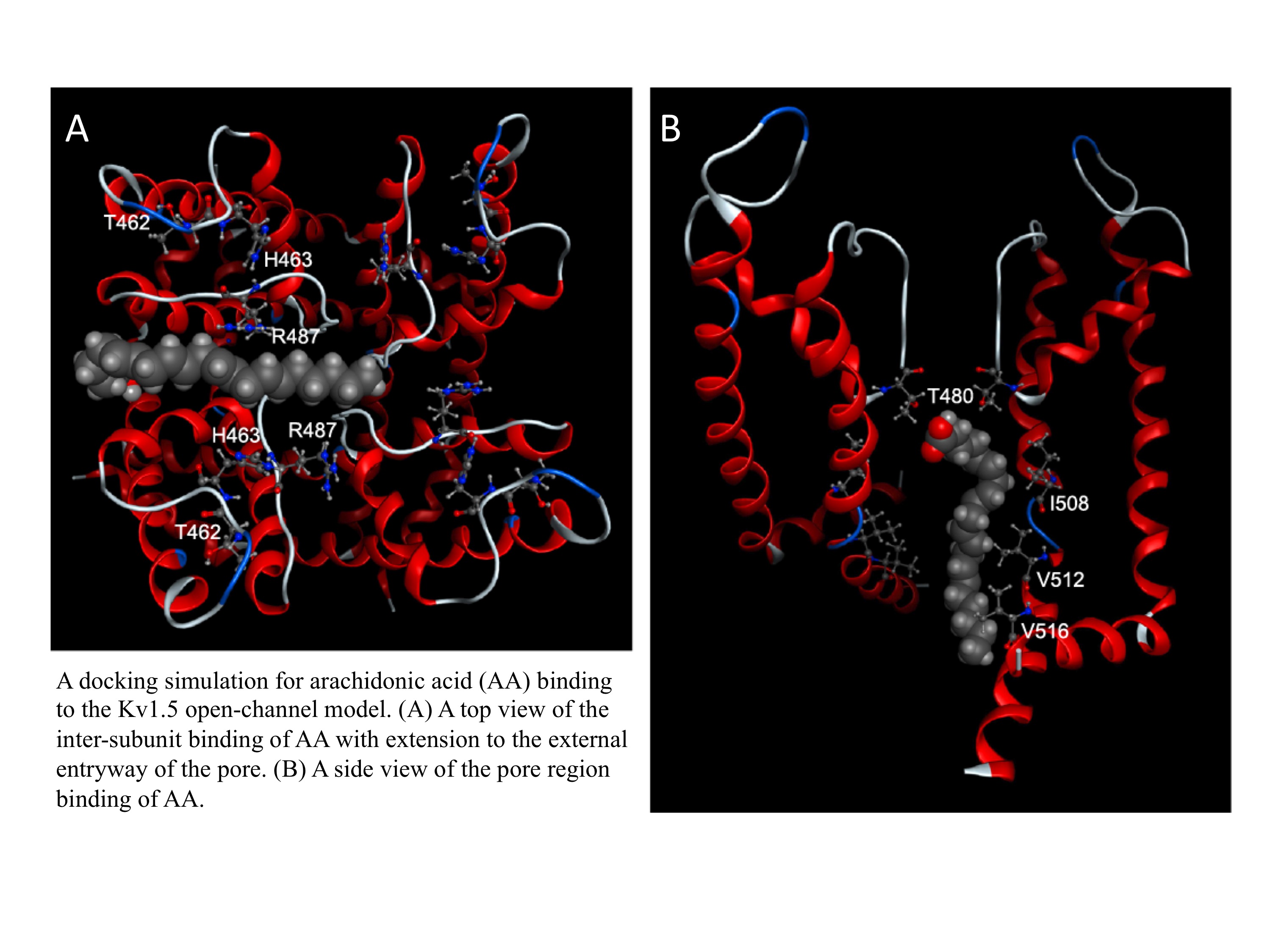 心筋K+チャネル(Kv1.5)は、ヒトでは主に心房筋に発現しており、活動電位の再分極過程を制御しています。私たちはKv1.5チャ
ネルの薬剤感受性を検討する目的でポア領域(P,イオンの通過領域)およびポアの構造に関わるS6領域のアミノ酸残基をアラニンに置き換えて(アラニンス
キャニング)種々の薬剤(Nisoldipine, Verapamil, Bepridil)や脂質(Docosahexaenoic acid,
DHA)とチャネルとの相互作用を調べています。一方、近年Kv1.5をコードする遺伝子の先天性変異や一塩基多型によりチャネル電流量の減少等を伴う機能障害(loss of function)が惹起され、結果として心房筋活動電位の再分極過程に異常をきたし心房細動の発症に関わることが示唆されています。よって私たちはKv1.5チャネルおよびその機能障害を伴う遺伝子変異体を用い、抗不整脈薬剤やprotein kinaseによるチャネルタンパク質の膜輸送への修飾についても調べています。
心筋K+チャネル(Kv1.5)は、ヒトでは主に心房筋に発現しており、活動電位の再分極過程を制御しています。私たちはKv1.5チャ
ネルの薬剤感受性を検討する目的でポア領域(P,イオンの通過領域)およびポアの構造に関わるS6領域のアミノ酸残基をアラニンに置き換えて(アラニンス
キャニング)種々の薬剤(Nisoldipine, Verapamil, Bepridil)や脂質(Docosahexaenoic acid,
DHA)とチャネルとの相互作用を調べています。一方、近年Kv1.5をコードする遺伝子の先天性変異や一塩基多型によりチャネル電流量の減少等を伴う機能障害(loss of function)が惹起され、結果として心房筋活動電位の再分極過程に異常をきたし心房細動の発症に関わることが示唆されています。よって私たちはKv1.5チャネルおよびその機能障害を伴う遺伝子変異体を用い、抗不整脈薬剤やprotein kinaseによるチャネルタンパク質の膜輸送への修飾についても調べています。文責: 林 維光(Wei-Guang Ding)
心臓ペースメーカー細胞における持続性内向きNa+電流(Ist)の分子実体の解明
心臓の拍動リズムを生み出すしくみは、生命に対する根源的な問いとして古くから生理学者を魅了してきました。心臓の律動は、わずか数千個ほどしかない ペースメーカー細胞(洞房結節細胞)によって支配されています。また、これらの細胞の自律的な興奮(電気活動)は、イオンチャネルやトランスポーターと呼 ばれる細胞膜の起電性分子が発生する微弱なイオン電流により支えられています。これらの知見の多くは、半世紀にもおよぶ精緻な電気現象の観察を通して築か れてきたものでありますが、分子的な背景が依然として不明な点も少なくありません。
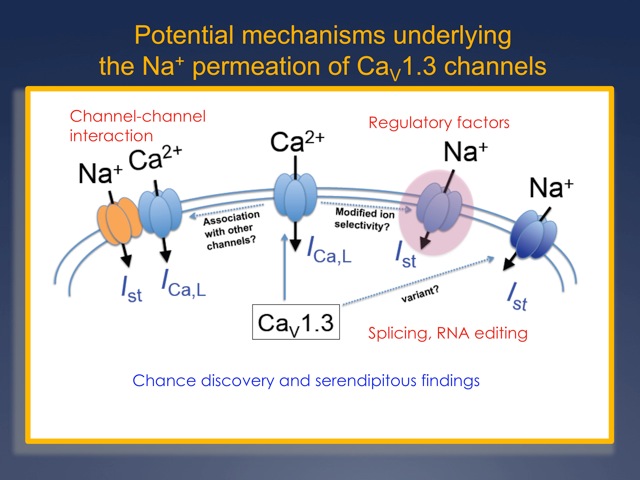
洞房結節細胞において特異的に発見された持続性内向きNa+電流(Ist)は、心拍リズムの形成に重要な役割を果たすことが示唆されているものの、この 電気現象を担うチャネル分子は未だは同定されていません。これまでに、私たちは、Istの分子解明の手がかりとなる様々な実験データを得てきています。そ こから、“L型Ca2+チャネル(CaV1.3)がNa+電流を担う”という未知の分子機構が仮説として浮かび上がってきました(図参照)。私たちは、こ の新しい可能性について様々な角度から検討し、Istの分子実体を明らかにするべく日々研究を進めています。
心臓のペースメーカー活動に関わる分子基盤の全容を解明することは、生命を脅かす様々な不整脈の発生メカニズムの理解、さらには心機能制御に向けた分子創薬など将来の幾多の試みの基礎になるものと考えています。
文責: 豊田 太(Futoshi Toyoda)
順次更新していきます

