インフルエンザウイルスに対するワクチンや抗ウイルス薬の開発
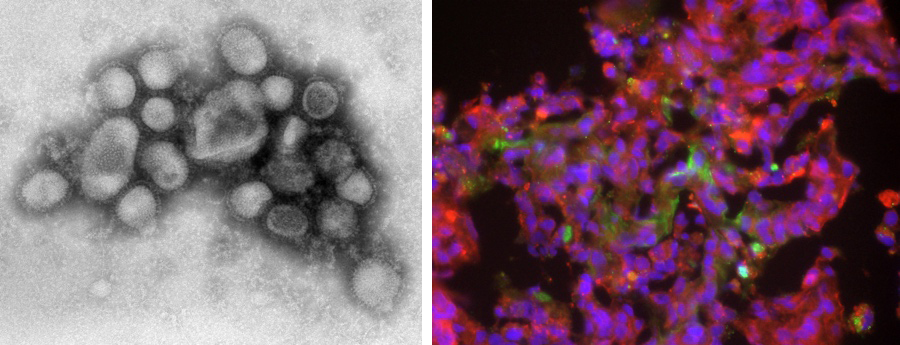
私達は、カニクイザルを用いて、2009年に世界的に流行したパンデミックH1N1インフルエンザウイルスの病原性解析を世界に先駆けて行いました (Nature 2009)。さらに、高病原性鳥インフルエンザウイルスの侵入が日本国内でも見られ、世界的に人の感染が報告されているので、人が感染した場合の重症化の原因を明らかにしたいと考えています。この問題を解決する為に、高病原性鳥インフルエンザウイルス感染によりカニクイザルが重症になる動物実験系を確立しました (Vaccine 2007; Virology 2016)。この系を用いて、インフルエンザウイルス感染によるカニクイザルが重症化する原因が徐々に明らかになってきています。
私達は北海道大学喜田宏教授の研究室で開発されたインフルエンザウイルスに対するワクチンの効果をマウスだけではなくカニクイザルを用いて研究しています。不活化法を改良した完全粒子ワクチンの有効性、安全性を検証し、現行のスプリットワクチンより有効であることを示しています (PLoS One 2012; Vaccine 2022)。
インフルエンザの治療薬の研究では、サルモデルを使い、既存薬や新規開発薬の有効性を検証しています。さらに動物モデルを使い、薬剤耐性ウイルスの出現頻度を予測し、耐性ウイルスの性状を解析しています(Antiviral Research 2020)。
病原性に関する論文
- Virology 606, 110511, 2025. doi.org/10.1016/j.virol.2025.110511
- Antiviral Research 178: 104790, 2020. doi.org/10.1016/j.antiviral.2020.104790
- Virology 493: 31-38, 2016. doi: 10.1016/j.virol.2016.03.007.
- PLOS One 8: e75910, 2013. doi.org/10.1371/journal.pone.0075910
- Virology 407: 178-184, 2010. doi:10.1016/j.virol.2010.08.006.
- Nature 460: 1021-1025, 2009. doi:10.1038/nature08260.
ワクチンに関する論文
- npj Vaccines 10: 164, 2025. https://www.nature.com/articles/s41541-025-01221-x
- Vaccine 40: 4026-4037, 2022. doi.org/10.1016/j.vaccine.2022.05.045
- Vaccine 35: 1008-1017, 2017. doi:10.1016/j.vaccine.2017.01.008.
- Scientific Reports 6: 37915, 2016. doi:10.1038/srep37915.
- Pathology International 66: 678-686, 2016. doi:10.1111/pin.12472.
- PLOS One 8: e82740, 2013. doi.org/10.1371/journal.pone.0082740
- PLOS One 7: e37220, 2012. doi.org/10.1371/journal.pone.0037220
- Vaccine 28: 780-789, 2010. doi:10.1016/j.vaccine.2009.10.067.
- J Med Primatol 39: 58-70, 2010. doi:10.1111/j.1600-0684.2009.00395.x.
- Vaccine 27: 7402-7408, 2009. doi:10.1016/j.vaccine.2009.08.089.
- Immunology 124: 155-165, 2008. doi:10.1111/j.1365-2567.2007.02745.x.
- Vaccine 26: 562-572, 2008. doi:10.1016/j.vaccine.2007.11.031.
- Vaccine 25: 4914-4921, 2007. doi:10.1016/j.vaccine.2007.04.010.
治療薬に関する論文
- Nature Communications, 12:2654, 2021. doi: 10.1038/s41467-021-22964-w
- Antimicrob Agents Chemother 65: e01825-20, 2021. doi: 10.1128/AAC.01825-20.
- Antimicrob Agents Chemother 64: e02561-19, 2020. doi: 10.1128/AAC.02561-19.
- Antiviral Research 178: 104790, 2020. doi.org/10.1016/j.antiviral.2020.104790.
- Antiviral Research 171: 104591, 2019. doi:10.1016/j.antiviral.2019.104591.
- Antimicrob Agents Chemother 59: 4962-4973, 2015. doi:10.1128/AAC.00793-15.
- PLOS Pathogens 10: e1004192, 2014. doi:10.1371/journal.ppat.1004192.
- Antimicrob Agents Chemother 58: 4795-4803, 2014. doi:10.1128/AAC.02817-14.
- Antimicrob Agents Chemother 55: 4961-4970, 2011. doi:10.1128/AAC.00412-11.
新型コロナウイルスの病態解明とワクチン・治療薬の開発
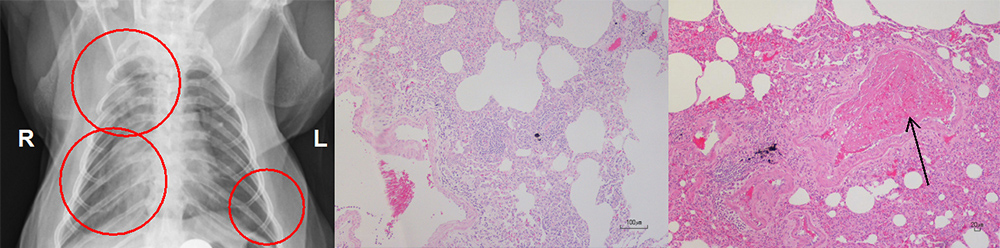
世界中に広がった新型コロナウイルス対策の研究を2020年より進めています。霊長類モデルを使い、新型コロナウイルスが肺炎を起こし、血栓を生じさせることを明らかにしました (Virology 2021)。霊長類モデルは人の病態と類似する点が多く、ワクチンや治療薬の開発に活用しています。霊長類モデルの肺炎の画像診断、病理解析、サルの免疫反応の測定、ウイルス量の測定、ウイルス遺伝子解析などを通して、ベクターワクチンやmRNAワクチンなど国産ワクチンの開発、実用化に必要な有効性を確認する実験を行っています(Frontiers Microbiol 2022; bioRxiv 2021)。
病原性に関する論文
- Virology 606, 110511, 2025. doi.org/10.1016/j.virol.2025.110511
- J Neuroimmunol 387:578228, 2024. doi.org/10.1016/j.jneuroim.2024.578288
- Virology 594:110052, 2024. doi.org/10.1016/j.virol.2024.110052
- Virology 554:97-105, 2021. doi.org/10.1016/j.virol.2020.12.013
ワクチンに関する論文
- Virology 616, 110778, 2026. doi.org/10.1016/j.virol.2025.110778
- Journal of Virology 99: e0229024, 2025. doi:106.10.1128/jvi.02290-24
- Frontiers in Microbiology 13:967019, 2022. https://www.frontiersin.org/articles/10.3389/fmicb.2022.967019/full
- bioRxiv. doi:doi.org/10.1101/2021.03.04.433852, posted march 04, 2021.
治療薬に関する論文
早期老化症候群と老化現象の分子機構の解明
加齢、老化に伴う代謝の変化、免疫反応の低下、腫瘍や自己免疫疾患の発生などのメカニズムを解明するために動物モデルを使い研究を進めています。ゲノム編集により早期老化症候群モデルカニクイザルを作成し、加齢現象を加速させ、生体変化を解析しています。
自己免疫疾患に関連する論文
腫瘍に対する免疫反応と治療薬の研究
私達の腫瘍免疫研究の特徴はカニクイザルを用いていることです。滋賀医科大学動物生命科学研究センターは、移植の際に拒絶反応の原因となる主要組織適合抗原複合体(Major histocompatibility complex, MHC)を解析し、特定のMHCを持つカニクイザルを繁殖維持しています。同一のMHC型を2個の染色体の両方に持つカニクイザル(MHCホモ接合サル)の細胞は、同じMHCを一方の染色体にだけもつカニクイザル(MHCヘテロ接合サル)に少ない拒絶反応で移植可能です。私達はこのサルを利用して、カニクイザルの癌細胞移植モデルを作成し、腫瘍に対する免疫反応を解析しています。
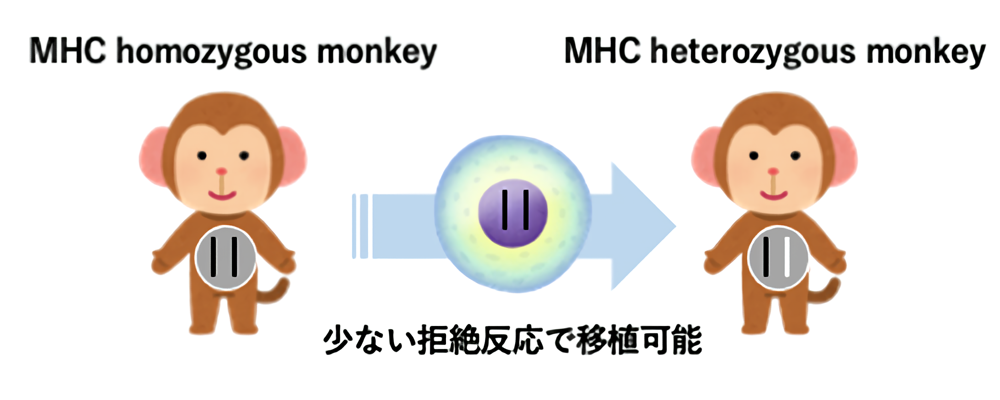
カニクイザルの癌細胞移植モデルの作成を行いました。MHCホモ接合サルの細胞から作製したiPS細胞を用い、様々な種類の癌細胞を作製しました。この癌細胞をMHC ヘテロ接合サルに移植することで、カニクイザル癌モデルの作製に取り組んでいます。胎児性癌細胞を移植したカニクイザルに、癌細胞表面上のGRP94に対する抗体ができ、癌は拒絶されました(Cancer Res 2017)。また移植した癌細胞の中に、癌細胞特異的なキラーT細胞(TIL)が浸潤していることも判明しました(Sci Rep 2020)。
現在、このTILが発現している抗原特異的なT細胞レセプター(T cell receptor, TCR)遺伝子をもち、癌細胞を攻撃できるT細胞を作製し、細胞治療を行う実験を、生化学・分子生物学講座 分子生理化学部門と共同で行っています(Molecular Therapy - Oncolytics 2022)。
腫瘍免疫に関する論文
- PLOS One 20, e0305153, 2025. doi.org/10.1371/journal.pone.0305153
- Molecular Therapy - Oncolytics 24:77-86, 2022. doi.org/10.1016/j.omto.2021.12.003
- Scientific Reports 21:8414, 2020. doi:10.1038/s41598-020-65488-x
- PLOS One 13: e0204745, 2018. doi:org/10.1371/journal.pone.0204745
- Cancer Research 77: 6001-6010, 2017. doi:10.1158/0008-5472.CAN-17-0775

 ホーム
ホーム