お知らせ
| [2025年5月27日] 2025年6月1日より、利益相反申告の一部をシステム申告に切り替えます。 システム申告の対象となる利益相反: 1.生命・医学系指針研究 2.治験 3.厚労科研 4.AMED 5.定期自己申告(2025年11月頃~予定) 学外分担者で、本学で利益相反審査を受ける必要のある方は、「様式2_学外分担者用(ヒト指針).xlsx」にご記入の上、学内研究者にご提出ください。 様式のダウンロードはこちら |
| 過去のお知らせはこちら |
利益相反ポリシー
- 国立大学法人滋賀医科大学利益相反ポリシー(令和4年3月24日改正)
- 国立大学法人滋賀医科大学組織的利益相反マネジメントポリシーPDF版
関係資料・規程
- 国立大学法人滋賀医科大学利益相反マネジメント規程(令和4年3月31日改正)
- 国立大学法人滋賀医科大学組織的利益相反マネジメント規則(令和4年8月3日改正)
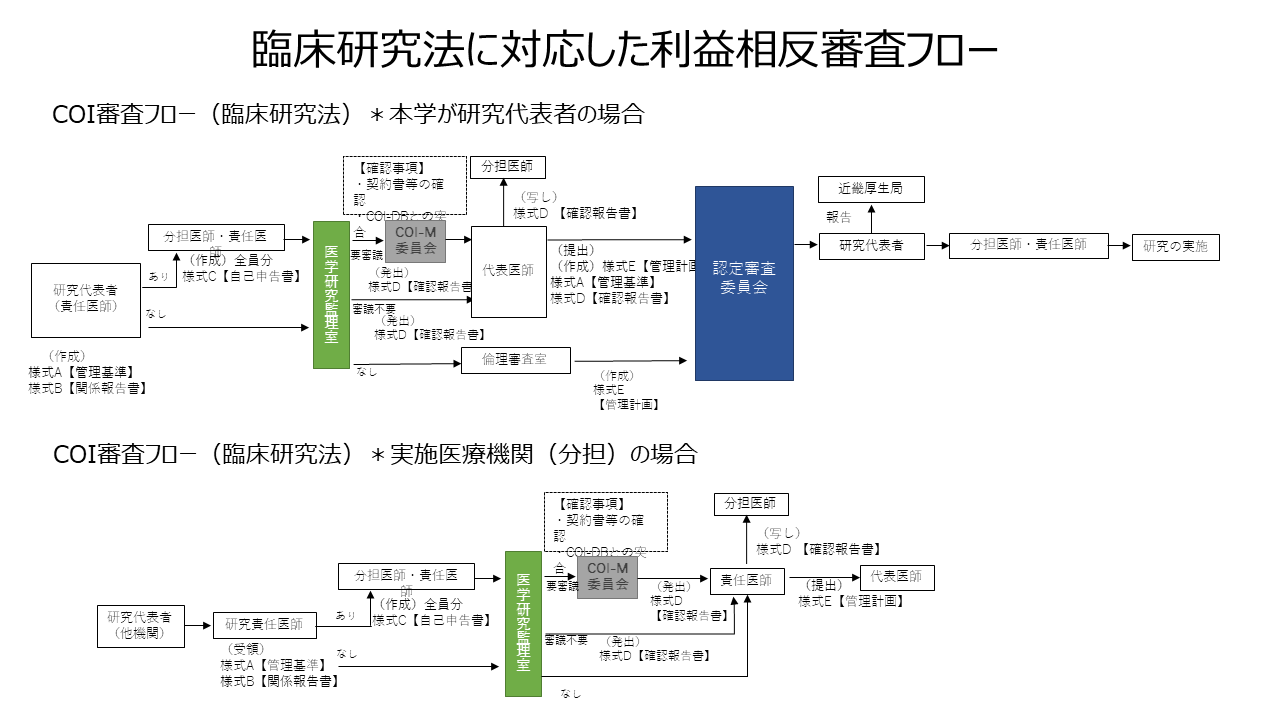
- 「臨床研究法における利益相反管理」資料(平成30年7月12日)
【臨床研究法に対応した利益相反審査】
相談・通報について
下記窓口までご相談ください。
相談窓口
利益相反マネジメント委員会事務局
TEL 077-548-2896(E-mail: hqcoi@belle.shiga-med.ac.jp)
